Hidrocarburos Aromáticos

- El benceno se aisló por primera vez en 1825 por Michael Faraday.
- La fórmula empírica del nuevo compuesto era CH. La síntesis de este compuesto se consiguió en 1834 por Eilhard Mistscherlich al calentar ácido benzoico, aislado de la goma de benjuí, en presencia de cal.
- En la última parte del siglo XIX se descubrieron muchos otros compuestos que parecían estar relacionados con el benceno pues tenían bajas relaciones hidrógeno/carbono y aromas agradables y por eso a este grupo de compuestos se les denominó hidrocarburos aromáticos.
- El término aromático se aplica en la actualidad a una serie de compuestos cuya estabilidad y reactividad es semejante a la del benceno, independientemente de su olor.
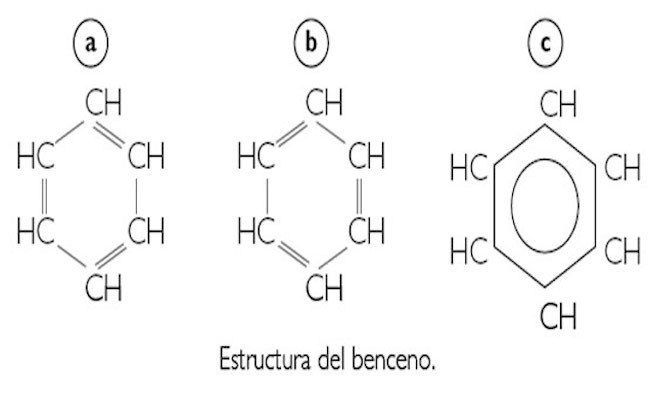

- Las estructuras de Kekulé satisfacen las condiciones para la resonancia. Son estructuras que solo difieren en la disposición de los e- . El benceno es un híbrido entre ambas estructuras de Kekulé.
- Las 36 kcal de energía que el benceno no libera se encuentra como energía de Resonancia y es la responsable de las propiedades aromáticas que presenta.
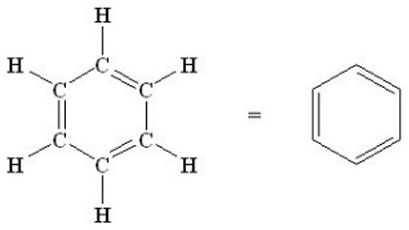
COMPUESTOS AROMÁTICOS
- Los hidrocarburos aromáticos son compuestos insaturados de un tipo especial. Originalmente recibieron el nombre de aromáticos debido al aroma que algunos poseen. Sin embargo no todos son odoríferos y muchos compuestos fragantes no son de tipo aromático.
- Uno de los compuestos más simples y que se conoció primero con la estructura especial característica de los compuestos aromáticos fue el hidrocarburo benceno.
- Los hidrocarburos aromáticos simples que se usan como material de partida para elaborar productos más complejos provienen de dos fuentes principales, el carbón (o hulla) y el petróleo.
- El carbón es una sustancia mineral enormemente compleja formada en mayor medida por grandes arreglos de anillos insaturados del tipo del benceno unidos entre sí.
- Son compuestos de baja polaridad.
- Insolubles en agua.
- Menos densos que el agua.
- Hasta no hace mucho y a pesar de su inflamabilidad, el benceno se usó ampliamente como disolvente. Este uso ha desaparecido prácticamente una vez que fue demostrado que el benceno es un cancerígeno. El tolueno ha reemplazado al benceno como disolvente orgánico barato, porque tiene propiedades similares como disolvente y no se ha demostrado que sea cancerígeno en los sistemas celulares y a los niveles que lo es el benceno.
Por medio de este tipo de reacción de sustitución electrofílica es posible introducir muchos sustituyentes distintos en el anillo aromático. Seleccionando las condiciones y los reactivos apropiados, el anillo aromático puede reaccionar de la siguiente forma:
Halogenación: El anillo aromático se puede halogenar (sustituir con un halógeno: -Cl, -Br) utilizando un catalizador que es un ácido de Lewis como FeBr3o FeCl3.La función del catalizador es generar el electrófilo Br+.
Nitración: El benceno experimenta nitración (sustituir con un grupo nitro: -NO2 ) cuando se trata con HNO3 concentrado. El ácido de Lewis catalizador en esta reacción es el H2SO4 concentrado.
Sulfonación: (sustituir con un grupo sulfónico: -SO3H) del benceno con ácido sulfúrico fumante (H2SO4 + SO3 ) produce un ácido bencensulfónico.
- Compuestos aromáticos: aquellos que son semejantes al benceno.
- Propiedades que presentan: contienen anillos aromáticos, alto grado de insaturación, sufren reacciones de sustitución electrofílica, son estables, bajos calores de combustión e hidrogenación, sustancias cíclicas (anillos de 5,6 y 7 átomos), moléculas planas.
- Sustancia aromática: sustancia cuya molécula debe tener nubes cíclicas de e- pi deslocalizados encima y debajo del plano de la molécula. Estas nubes pi deben contener un total de (4n+2) e - pi (Regla de Hückel)
NOMENCLATURA

Todo benceno disustituido tiene tres isómeros constitucionales, y existen dos métodos aceptables para escribir la orientación relativa de los sustituyentes: mediante el uso de números de posición relativa, y empleando las designaciones orto, meta y para que se suelan abreviar como o, m y p.
- Si muchos grupos están enlazados al anillo bencénico, debemos no sólo decir cuales son, sino también indicar sus posiciones relativas.
- Un benceno disustituido puede tener tres isómeros, los cuales se diferencian entre sí por el uso de los prefijos orto (o- ), meta (m-) y para (p-).
- Líquido de olor agradable.
- Muy volátil.
- Menos denso que el agua.
- Insoluble en agua pero soluble en compuestos orgánicos.
- Sufre reacciones típicas de Sustitución electrofílica como la halogenación, nitración, sulfonación y alquilación.
- Las reacciones de adición, como la hidrogenación, se producen solo en presencia de catalizadores y a alta temperatura.
- Grupos activadores: donan carga al anillo, lo hacen más negativo y más reactivo que el benceno. Orientan a la posición orto-para.
- Grupos desactivadores: toman carga del anillo y lo hace menos reactivo que el benceno. Orienta posición meta (excepto los halógenos, directores orto-para).
HETEROCICLOS AROMÁTICOS
- Piridina tiene 32 kcal/mol de energía de resonancia, ligeramente menor que la del benceno.
- De los dos orbitales con dos pares de electrones del átomo de oxígeno en le furano, uno forma parte del sestete aromático y el otro no.
- La energía de resonancia del furano es 16 kcal/mol.
- Son compuestos aromáticos formados de dos o más anillos aromáticos.
- El naftaleno es el hidrocarburo aromático polinuclear más simple. Otros son el antraceno y el fenantreno.
Un hidrocarburo aromático polinuclear es un hidrocarburo compuesta de condensados aromáticos moléculas de anillo. Estos son anillos que comparten uno o más lados y contienen electrones deslocalizados. Otra forma de considerar PAHs es moléculas hechas por la fusión de dos o más anillos de benceno.













Buen trabajo
ResponderEliminar